Πλαίσιο: Η βάση αποδεικτικών στοιχείων για τη θεραπευτική αντιμετώπιση του Covid-19 αυξάνεται με πολυάριθμες τυχαιοποιημένες ελεγχόμενες δοκιμές (RCT) σε εξέλιξη. Αυτή η ενημέρωση περιλαμβάνει συστάσεις για το πλάσμα ανάρρωσης, οι οποίες βασίζονται σε συγκεντρωτικά δεδομένα από 16 RCT με 16.236 ασθενείς.
Νέες συστάσεις: Η Ομάδα Ανάπτυξης Κατευθυντήριων Γραμμών (GDG) έκανε ισχυρή σύσταση κατά της χρήσης πλάσματος ανάρρωσης σε ασθενείς με μη σοβαρή ασθένεια και σύσταση κατά της χρήσης του σε ασθενείς με σοβαρή και κρίσιμη ασθένεια, εκτός από το πλαίσιο RCT.
Κατανόηση των νέων συστάσεων: Κατά τη μετάβαση από τα στοιχεία σε συστάσεις κατά της χρήσης πλάσματος ανάρρωσης, η GDG εξέτασε έναν συνδυασμό αποδεικτικών στοιχείων που αξιολογούν σχετικά οφέλη και βλάβες, αξίες και προτιμήσεις και ζητήματα σκοπιμότητας. Η GDG αναγνώρισε ότι δεν υπήρχε σαφές όφελος για κρίσιμα αποτελέσματα όπως η θνησιμότητα και ο μηχανικός αερισμός για ασθενείς με μη σοβαρή, σοβαρή ή κρίσιμη ασθένεια και σημαντικές απαιτήσεις πόρων όσον αφορά το κόστος και τον χρόνο χορήγησης. Έτσι, η ισχυρή σύσταση κατά της χρήσης αντικατοπτρίζει την άποψη της GDG ότι η χορήγηση πλάσματος, ειδικά για ασθενείς με μη σοβαρή ασθένεια όπου υπάρχει χαμηλός αρχικός κίνδυνος θνησιμότητας και άλλα σημαντικά κλινικά αποτελέσματα, δεν δικαιολογείται. Η GDG πίστευε ότι, παρόλο που το πλάσμα που αναρρώνει δεν θα πρέπει να χρησιμοποιείται σε υποομάδες βαρύτητας ως μέρος της τακτικής φροντίδας,
Προηγούμενες συστάσεις:
Συνιστάται για ασθενείς με σοβαρό και κρίσιμο COVID-19:
- μια ισχυρή σύσταση για συστηματικά κορτικοστεροειδή.
- μια ισχυρή σύσταση για αναστολείς των υποδοχέων IL-6 (τοσιλιζουμάμπη ή σαριλουμάμπη).
- μια υπό όρους σύσταση για το casirivimab και το imdevimab, για όσους έχουν οροαρνητικό καθεστώς.
Συνιστάται για ασθενείς με μη σοβαρό COVID-19:
- μια υπό όρους σύσταση για το casirivimab και το imdevimab, για όσους διατρέχουν τον υψηλότερο κίνδυνο σοβαρής νόσου.
Δεν συνιστάται για ασθενείς με μη σοβαρό COVID-19:
- μια υπό όρους σύσταση κατά των συστηματικών κορτικοστεροειδών.
Δεν συνιστάται, ανεξάρτητα από τη σοβαρότητα της νόσου COVID-19
- μια υπό όρους σύσταση κατά της ρεμδεσιβίρης.
- μια ισχυρή σύσταση κατά της υδροξυχλωροκίνης.
- μια ισχυρή σύσταση έναντι της λοπιναβίρης/ριτοναβίρης.
- μια σύσταση κατά της ιβερμεκτίνης, εκτός από το πλαίσιο μιας κλινικής δοκιμής.
Σχετικά με αυτήν την κατευθυντήρια γραμμή: Αυτή η ζωντανή κατευθυντήρια γραμμή, από τον Παγκόσμιο Οργανισμό Υγείας (ΠΟΥ), ενσωματώνει νέες συστάσεις για θεραπείες για τον COVID-19 και παρέχει ενημερώσεις για τις υπάρχουσες συστάσεις. Η GDG συνήθως αξιολογεί ένα φάρμακο όταν ο ΠΟΥ κρίνει ότι υπάρχουν επαρκή στοιχεία για να κάνει μια σύσταση. Ενώ η GDG λαμβάνει μια ατομική οπτική γωνία για τον ασθενή κατά τη διατύπωση συστάσεων, εξετάζει επίσης τις επιπτώσεις των πόρων, την αποδοχή, τη σκοπιμότητα, την ισότητα και τα ανθρώπινα δικαιώματα. Αυτή η κατευθυντήρια γραμμή αναπτύχθηκε σύμφωνα με πρότυπα και μεθόδους για αξιόπιστες οδηγίες. Υποστηρίζεται από ζωντανές συστηματικές ανασκοπήσεις με δικτυακές μετα-αναλύσεις (LNMA) [1] [2] [3] .
Ενημερώσεις και πρόσβαση: Αυτή είναι η έβδομη ενημέρωση της ζωντανής κατευθυντήριας γραμμής, που αντικαθιστά προηγούμενες εκδόσεις. Η τρέχουσα κατευθυντήρια γραμμή και οι προηγούμενες εκδόσεις της είναι διαθέσιμες μέσω του ιστότοπου του ΠΟΥ [4] , του BMJ [5] και του MAGICapp (διαδικτυακά και επίσης ως έξοδοι PDF για αναγνώστες με περιορισμένη πρόσβαση στο Διαδίκτυο). Η κατευθυντήρια γραμμή διαβίωσης συντάσσεται, διαδίδεται και ενημερώνεται σε μια διαδικτυακή πλατφόρμα (MAGICapp), με φιλική προς το χρήστη μορφή και εύκολη στην πλοήγηση δομή που φιλοξενεί δυναμικά ενημερωμένα στοιχεία και συστάσεις, εστιάζοντας σε ό,τι είναι νέο, διατηρώντας παράλληλα τις υπάρχουσες συστάσεις εντός των κατευθυντήρια γραμμή. Αυτή η ζωντανή κατευθυντήρια γραμμή του ΠΟΥ για τις θεραπείες για τον COVID-19 σχετίζεται με τη μεγαλύτερη, πιο ολοκληρωμένη οδηγία για Κλινική διαχείριση COVID-19 [6] . Οδηγίες για τη χρήση φαρμάκων για την πρόληψη (αντί για τη θεραπεία) του COVID-19 δημοσιεύονται χωριστά στον ιστότοπο του ΠΟΥ [7] και στο BMJ [8] , που υποστηρίζεται από ένα LNMA [9] .
Μέχρι τις 10 Νοεμβρίου 2021, υπήρχαν πάνω από 251 εκατομμύρια επιβεβαιωμένα κρούσματα COVID-19 [10] . Η πανδημία έχει μέχρι στιγμής στοιχίσει περισσότερες από 5,1 εκατομμύρια ζωές [10] . Ο εμβολιασμός έχει ουσιαστικό αντίκτυπο στον αριθμό των κρουσμάτων και τις νοσηλείες σε ορισμένες χώρες υψηλού εισοδήματος, αλλά οι περιορισμοί στην παγκόσμια πρόσβαση στα εμβόλια σημαίνουν ότι πολλοί πληθυσμοί παραμένουν ευάλωτοι [10] [11] . Ακόμη και σε εμβολιασμένα άτομα, παραμένουν αβεβαιότητες σχετικά με τη διάρκεια της προστασίας και την αποτελεσματικότητα των τρεχόντων εμβολίων κατά των αναδυόμενων παραλλαγών του SARS-CoV-2.
Συνολικά, εξακολουθεί να υπάρχει ανάγκη για πιο αποτελεσματικές θεραπείες για τον COVID-19. Η πανδημία του COVID-19 – και η έκρηξη τόσο της έρευνας όσο και της παραπληροφόρησης – έχει τονίσει την ανάγκη για αξιόπιστη, προσβάσιμη και τακτικά ενημερωμένη καθοδήγηση διαβίωσης για να τοποθετηθούν τα αναδυόμενα ευρήματα στο πλαίσιο και να παρέχονται σαφείς συστάσεις για την κλινική πρακτική [12] .
Αυτή η ζωντανή κατευθυντήρια γραμμή ανταποκρίνεται στα αναδυόμενα στοιχεία από τις RCT σχετικά με υπάρχουσες και νέες φαρμακευτικές θεραπείες για τον COVID-19. Περισσότερες από 5070 δοκιμές που διερευνούν παρεμβάσεις για τον COVID-19 έχουν καταγραφεί ή βρίσκονται σε εξέλιξη (βλ. Ενότητα 9 για αναδυόμενα στοιχεία) [13]. Μεταξύ αυτών είναι μεγάλες εθνικές και διεθνείς δοκιμές πλατφόρμας (όπως RECOVERY, WHO SOLIDARITY, REMAP-CAP και ACTIV) που προσλαμβάνουν μεγάλο αριθμό ασθενών σε πολλές χώρες, με ρεαλιστικό και προσαρμοστικό σχεδιασμό [14] [15] [16] [ 17] . Αυτές οι δοκιμές πλατφόρμας διερευνούν επί του παρόντος και αναφέρουν πολυάριθμες παρεμβάσεις, συμπεριλαμβανομένων αντιιικών μονοκλωνικών αντισωμάτων και ανοσοτροποποιητών. Αυτό το ταχέως εξελισσόμενο τοπίο αποδεικτικών στοιχείων απαιτεί αξιόπιστη ερμηνεία και κατευθυντήριες γραμμές ταχείας κλινικής πρακτικής για την ενημέρωση των κλινικών ιατρών και των υπευθύνων λήψης αποφάσεων υγειονομικής περίθαλψης.
Αυτή η έβδομη έκδοση της κατευθυντήριας γραμμής για τη ζωή του ΠΟΥ ασχολείται με τη χρήση πλάσματος ανάρρωσης σε δύο ομάδες ασθενών: σε αυτούς με μη σοβαρό COVID-19 και σε αυτούς με σοβαρή και κρίσιμη ασθένεια. Ακολουθεί τη διαθεσιμότητα 16 RCT και στις δύο ομάδες ασθενών, με βάση ένα LNMA για αντισώματα και κυτταρικές θεραπείες για τον COVID-19 [2] . Η χορήγηση πλάσματος ανάρρωσης περιλαμβάνει τη μεταφορά ενδογενώς παραγόμενων εξουδετερωτικών αντισωμάτων στο πλάσμα από ασθενείς που είχαν μολυνθεί προηγουμένως και έχουν αναρρώσει σε ασθενείς με ενεργή λοίμωξη.
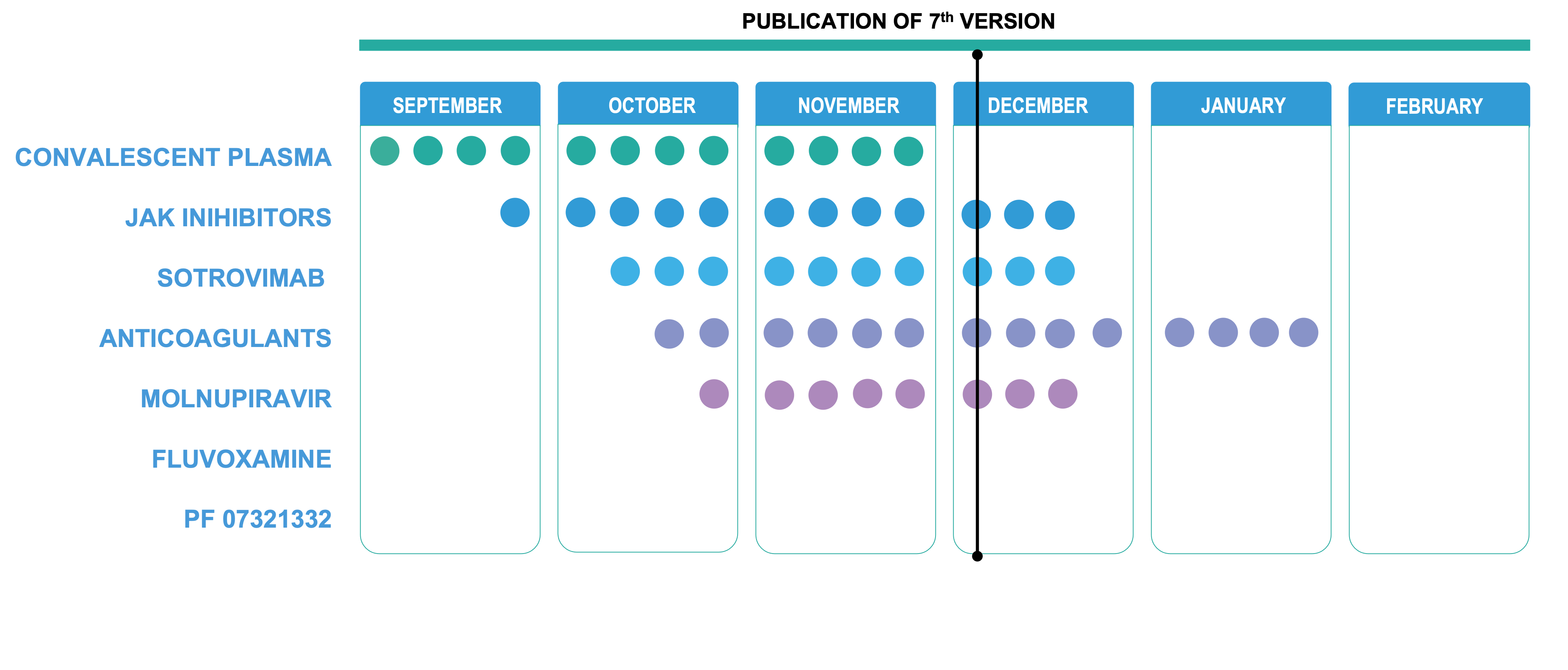
Το Σχ. 1 δείχνει άλλες θεραπευτικές αγωγές σε εξέλιξη για αυτήν την κατευθυντήρια γραμμή του ΠΟΥ για διαβίωση, που κοινοποιούνται επίσης μέσω της πύλης του ΠΟΥ [4] . Όταν αποφασίζει ποιες θεραπείες θα καλύψει, ο ΠΟΥ λαμβάνει υπόψη παράγοντες όπως η ύπαρξη σημαντικού όγκου αποδεικτικών στοιχείων για την πληροφόρηση των συστάσεων, και κρίνει εάν και πότε ενδέχεται να αναμένονται πρόσθετα στοιχεία. Ο ΠΟΥ διαθέτει μια μόνιμη διευθύνουσα επιτροπή (βλ. Ενότητα 10) για την αξιολόγηση νέων φαρμάκων και την ενημέρωση των υφιστάμενων συστάσεων.
Σχήμα 1. Θεραπευτικές ουσίες για τον COVID-19 υπό αξιολόγηση
Η κατευθυντήρια γραμμή για τη θεραπεία του COVID-19 ισχύει για όλους τους ασθενείς με COVID-19. Ωστόσο, για ορισμένα φάρμακα οι συστάσεις μπορεί να διαφέρουν για διαφορετικούς πληθυσμούς ασθενών, για παράδειγμα, με βάση τη σοβαρότητα της νόσου COVID-19. Η GDG χρησιμοποίησε τους ορισμούς της σοβαρότητας του ΠΟΥ με βάση κλινικούς δείκτες, προσαρμοσμένους από την κατηγοριοποίηση της σοβαρότητας της νόσου COVID-19 του ΠΟΥ (βλ. παρακάτω) [6] . Αυτοί οι ορισμοί αποφεύγουν την εξάρτηση από την πρόσβαση στην υγειονομική περίθαλψη για τον καθορισμό υποομάδων ασθενών.
Ορισμοί σοβαρότητας του ΠΟΥ
- Κρίσιμος COVID-19 – Καθορίζεται από τα κριτήρια για το σύνδρομο οξείας αναπνευστικής δυσχέρειας (ARDS), τη σήψη, το σηπτικό σοκ ή άλλες καταστάσεις που κανονικά θα απαιτούσαν την παροχή θεραπειών διατήρησης της ζωής, όπως μηχανικός αερισμός (επεμβατικός ή μη επεμβατικός) ή αγγειοκατασταλτικός θεραπεία.
- Σοβαρός COVID-19 – Ορίζεται από οποιοδήποτε από τα εξής:
- κορεσμός οξυγόνου < 90% στον αέρα του δωματίου.
- σε ενήλικες, σημεία σοβαρής αναπνευστικής δυσχέρειας (χρήση βοηθητικών μυών, αδυναμία ολοκλήρωσης πλήρους προτάσεων, αναπνευστικός ρυθμός > 30 αναπνοές ανά λεπτό) και, σε παιδιά, πολύ σοβαρή έλξη του θωρακικού τοιχώματος, γρύλισμα, κεντρική κυάνωση ή παρουσία οποιασδήποτε άλλης γενικής σημεία κινδύνου (αδυναμία θηλασμού ή ποτού, λήθαργος ή μειωμένο επίπεδο συνείδησης, σπασμοί) εκτός από τα σημάδια πνευμονίας.
- Μη σοβαρός COVID-19 – Ορίζεται ως η απουσία κριτηρίων για σοβαρό ή κρίσιμο COVID-19.
Προσοχή: Η GDG σημείωσε ότι το όριο κορεσμού οξυγόνου του 90% για τον ορισμό του σοβαρού COVID-19 ήταν αυθαίρετο και θα πρέπει να ερμηνεύεται προσεκτικά όταν χρησιμοποιείται για τον καθορισμό της σοβαρότητας της νόσου. Για παράδειγμα, οι κλινικοί γιατροί πρέπει να χρησιμοποιούν την κρίση τους για να προσδιορίσουν εάν ένας χαμηλός κορεσμός οξυγόνου είναι σημάδι σοβαρότητας ή είναι φυσιολογικός για έναν δεδομένο ασθενή με χρόνια πνευμονική νόσο. Ομοίως, ένας κορεσμός 90–94% στον αέρα του δωματίου είναι μη φυσιολογικός (σε ασθενή με φυσιολογικούς πνεύμονες) και μπορεί να είναι πρώιμο σημάδι σοβαρής νόσου, εάν ο ασθενής έχει πτωτική τάση. Γενικά, εάν υπάρχει αμφιβολία, η GDG πρότεινε να γίνει λάθος θεωρώντας την ασθένεια ως σοβαρή.
Το γράφημα απεικονίζει αυτές τις τρεις ομάδες σοβαρότητας της νόσου και βασικά χαρακτηριστικά που πρέπει να εφαρμόζονται στην πράξη.
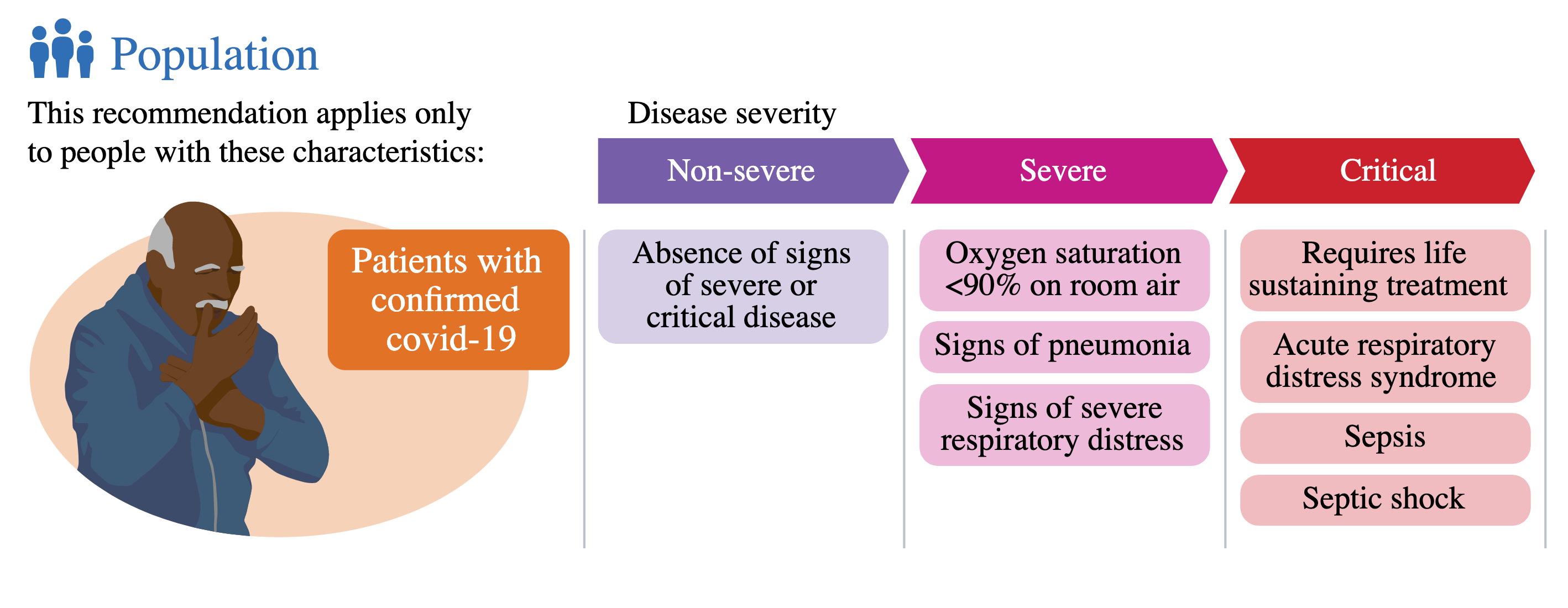
Infographic συμπαραγωγή των BMJ και MAGIC. σχεδιαστής Will Stahl-Timmins (βλ. BMJ Rapid Recommendations ).
Πλάσμα ανάρρωσης
Για ασθενείς με μη σοβαρό COVID-19 (που δεν πληρούν τα κριτήρια για σοβαρή ή κρίσιμη λοίμωξη): Συνιστούμε να μην χορηγείται πλάσμα ανάρρωσης για τη θεραπεία του COVID-19. (Ισχυρή σύσταση κατά).
Για ασθενείς με σοβαρό ή κρίσιμο COVID-19: Μόνο σε ερευνητικά πλαίσια. Συνιστούμε να μην χρησιμοποιείτε πλάσμα ανάρρωσης για τη θεραπεία του COVID-19, παρά μόνο στο πλαίσιο μιας κλινικής δοκιμής. (Συνιστάται μόνο σε ερευνητικά περιβάλλοντα).
Μηχανισμός δράσης










.jpg)










Για ασθενείς με σοβαρό ή κρίσιμο COVID-19 : Υπό όρους σύσταση. Προτείνουμε θεραπεία με casirivimab και imdevimab, υπό την προϋπόθεση ότι ο ασθενής έχει οροαρνητική κατάσταση. (Υπό όρους σύσταση για).
Μηχανισμός δράσης
Το Casirivimab και το imdevimab είναι δύο πλήρως ανθρώπινα αντισώματα (REGN10933 και REGN10987). Ο μηχανισμός δράσης τους είναι πολύ εύλογος: συνδέονται με την πρωτεΐνη ακίδας SARS-CoV-2 [48] και έχουν επιδείξει αντιική δράση σε μακάκους rhesus και συριακούς χρυσούς χάμστερ [49] . Τα φαρμακοκινητικά δεδομένα σε ασθενείς με μη σοβαρό COVID-19 δείχνουν ότι οι αντιικές συγκεντρώσεις και των δύο αντισωμάτων επιτυγχάνονται και διατηρούνται για τουλάχιστον 28 ημέρες μετά την ενδοφλέβια χορήγηση του συνδυασμού σε συνολική δόση 1200 mg (600 mg κάθε αντίσωμα) ή μεγαλύτερη [ 42] . Οι αντιιικές συγκεντρώσεις επιτυγχάνονται επίσης και διατηρούνται χρησιμοποιώντας υποδόρια συνολική δόση 1200 mg (600 mg κάθε αντισώματος) σε μη μολυσμένα άτομα για προφύλαξη [42] . Ο χρόνος ημιζωής κυμαίνεται από 25 έως 37 ημέρες και για τα δύο αντισώματα. Επί του παρόντος δεν είναι διαθέσιμα δεδομένα για τη φαρμακοκινητική του casirivimab και του imdevimab σε σοβαρό και κρίσιμο COVID-19, τα οποία είναι σημαντικά επειδή οι συγκεντρώσεις στον ορό άλλων μονοκλωνικών αντισωμάτων έχουν αναφερθεί ότι είναι χαμηλότερες κατά τη συστηματική φλεγμονή και συσχετίζονται με τα επίπεδα λευκωματίνης και CRP [50] . Τα διαθέσιμα δεδομένα υποδηλώνουν επίσης ότι όταν παραδίδονται σε συνδυασμό, η δραστηριότητα παραμένει για τις τρέχουσες κυκλοφορούσες παραλλαγές ανησυχίας [51] .
Αν και ο μηχανισμός είναι εύλογος, υποστηρίχθηκε ότι η χορήγηση μπορεί να έχει διαφορετικά αποτελέσματα σε ασθενείς που έχουν παραγάγει τα δικά τους αντισώματα πρωτεΐνης κατά του SARS-CoV-2 (εφεξής οροθετικά) σε σύγκριση με εκείνους που δεν έχουν (εφεξής οροαρνητικός). Υποτέθηκε ότι τα αποτελέσματα μπορεί να είναι μεγαλύτερα ή να περιορίζονται σε οροαρνητικά άτομα που δεν έχουν ακόμη αναπτύξει αποτελεσματική απόκριση αντισωμάτων.
Αναστολείς υποδοχέων IL-6 (δημοσιεύθηκε στις 6 Ιουλίου 2021)
Η σύσταση σχετικά με τους αναστολείς των υποδοχέων IL-6 (tocilizumab ή sarilumab) δημοσιεύθηκε στις 6 Ιουλίου 2021 ως η πέμπτη έκδοση της κατευθυντήριας γραμμής του ΠΟΥ για τη ζωή και στο BMJ ως Ταχείες Συστάσεις . Ακολούθησε τη δημοσίευση των δημοσιεύσεων των δοκιμών RECOVERY και REMAP-CAP τον Φεβρουάριο του 2021 και νέα δεδομένα δοκιμών από 1020 ασθενείς που τυχαιοποιήθηκαν τυχαιοποιημένα είτε με tocilizumab είτε με sarilumab στο REMAP-CAP, τα οποία διατέθηκαν στον ΠΟΥ την 1η Ιουνίου 2021.
Δεν έγιναν αλλαγές για τη σύσταση αναστολέα υποδοχέα IL-6 σε αυτήν την έβδομη έκδοση της κατευθυντήριας γραμμής.
Για ασθενείς με σοβαρό και κρίσιμο COVID-19
Τα κορτικοστεροειδή είχαν προηγουμένως συσταθεί ανεπιφύλακτα σε ασθενείς με σοβαρό και κρίσιμο COVID-19 [4] και συνιστούμε στους ασθενείς που πληρούν αυτά τα κριτήρια σοβαρότητας να λαμβάνουν τώρα τόσο κορτικοστεροειδή όσο και αναστολείς των υποδοχέων IL-6.
Μηχανισμός δράσης
Η IL-6 είναι μια πλειοτροπική κυτοκίνη που ενεργοποιεί και ρυθμίζει την ανοσολογική απόκριση στις λοιμώξεις. Οι αυξημένες συγκεντρώσεις IL-6 σχετίζονται με σοβαρά αποτελέσματα στον COVID-19, συμπεριλαμβανομένης της αναπνευστικής ανεπάρκειας και του θανάτου, αν και ο ρόλος της IL-6 στην παθογένεση της νόσου είναι ασαφής.
Το tocilizumab και το sarilumab είναι μονοκλωνικά αντισώματα εγκεκριμένα για χρήση στη ρευματοειδή αρθρίτιδα. Ανταγωνίζονται τις δεσμευμένες στη μεμβράνη και τις διαλυτές μορφές του υποδοχέα IL-6 (IL-6R/sIL-6R). Το tocilizumab έχει εγκριθεί για ενδοφλέβια χρήση στη ρευματοειδή αρθρίτιδα και το sarilumab για υποδόρια χρήση, αν και στον COVID-19 και τα δύο έχουν μελετηθεί ενδοφλεβίως. Στις δόσεις που μελετήθηκαν στο COVID-19, και τα δύο φάρμακα αναμένεται να επιτύχουν πολύ υψηλά επίπεδα κατάληψης υποδοχέων με βάση μελέτες στη ρευματοειδή αρθρίτιδα [29]. IL-6 inhibitors are being repurposed in terms of indication but not in terms of the primary pharmacological mechanism of action. Efficacy in COVID-19 depends upon the importance of IL-6 signalling in the pathophysiology of the disease, rather than upon whether the doses used achieve target concentrations.
Ιβερμεκτίνη (δημοσιεύθηκε στις 31 Μαρτίου 2021)
Η σύσταση σχετικά με την ιβερμεκτίνη δημοσιεύθηκε στις 31 Μαρτίου 2021 ως η τέταρτη έκδοση της κατευθυντήριας γραμμής του ΠΟΥ για τη ζωή και στο BMJ ως Ταχείες Συστάσεις . Ακολούθησε την αυξημένη διεθνή προσοχή στην ιβερμεκτίνη ως πιθανή θεραπευτική επιλογή.
Δεν έγιναν αλλαγές για τη σύσταση της ιβερμεκτίνης σε αυτήν την έβδομη έκδοση της κατευθυντήριας γραμμής. Γνωρίζουμε για μερικές νέες, σχετικά μικρές δοκιμές που δημοσιεύθηκαν από τότε που έγινε η σύστασή μας και ότι έκτοτε ανακλήθηκε μία βασική δοκιμή λόγω ανησυχιών σχετικά με την απάτη στην έρευνα [54] [55] . Ωστόσο, η ενημερωμένη περίληψη αποδεικτικών στοιχείων από το LNMA είναι συνεπής με τη σύστασή μας που είχαμε κάνει στο παρελθόν. Αυτή η ενημερωμένη περίληψη αποδεικτικών στοιχείων θα εξεταστεί πλήρως από τη GDG πριν από την επόμενη επανάληψη αυτής της κατευθυντήριας γραμμής.
Παρατήρηση: Αυτή η σύσταση ισχύει για ασθενείς με οποιαδήποτε σοβαρότητα ασθένειας και οποιαδήποτε διάρκεια συμπτωμάτων.
Μια σύσταση για χρήση ενός φαρμάκου μόνο στο πλαίσιο κλινικών δοκιμών είναι κατάλληλη όταν υπάρχουν στοιχεία πολύ χαμηλής βεβαιότητας και η μελλοντική έρευνα έχει μεγάλες δυνατότητες μείωσης της αβεβαιότητας σχετικά με τις επιπτώσεις της παρέμβασης και για να γίνει αυτό με λογικό κόστος.
Μηχανισμός δράσης
Η ιβερμεκτίνη είναι ένας αντιπαρασιτικός παράγοντας που παρεμβαίνει στη λειτουργία των νεύρων και των μυών των ελμίνθων μέσω της δέσμευσης διαύλων χλωρίου που καλύπτονται από γλουταμικό [68] . Με βάση πειράματα in vitro, ορισμένοι υποστήριξαν ότι η ιβερμεκτίνη μπορεί να έχει άμεση αντιική δράση κατά του SARS-CoV-2. Ωστόσο, στους ανθρώπους οι συγκεντρώσεις που απαιτούνται για την in vitro αναστολή είναι απίθανο να επιτευχθούν με τις δόσεις που προτείνονται για το COVID-19 [69] [70] [71] . Η ιβερμεκτίνη δεν είχε καμία επίδραση στο ιικό RNA του SARS-CoV-2 στο μοντέλο συριακού χρυσού χάμστερ της λοίμωξης SARS-CoV-2 [72]. Ο προτεινόμενος μηχανισμός παραμένει ασαφής: πολλαπλοί στόχοι έχουν προταθεί με βάση είτε την αναλογία με άλλους ιούς με πολύ διαφορετικούς κύκλους ζωής, είτε, όπως πολλές εκατοντάδες άλλοι υποψήφιοι, προσομοιώσεις που υποδεικνύουν μοριακή σύνδεση με πολλαπλούς ιικούς στόχους συμπεριλαμβανομένων των spike, RdRp και 3CLpro [73] [ 73] 74] [75] [76] [77] . Δεν υπάρχουν επί του παρόντος άμεσες ενδείξεις για οποιονδήποτε μηχανισμό αντιϊκής δράσης κατά του SARS-CoV-2.
Ορισμένοι έχουν προτείνει, βασιζόμενοι κυρίως σε έρευνες για άλλες ενδείξεις, ότι η ιβερμεκτίνη έχει ανοσοτροποποιητική δράση, αλλά και πάλι ο μηχανισμός παραμένει ασαφής. Ιστορικά δεδομένα έδειξαν ότι η ιβερμεκτίνη βελτίωσε την επιβίωση σε ποντίκια που έλαβαν μια θανατηφόρα δόση λιποπολυσακχαρίτη [78], και έχει οφέλη σε μοντέλα ποντικών ατοπικής δερματίτιδας και αλλεργικού άσθματος [79] [80] . Για τον SARS-CoV-2, μια υπόθεση υποδηλώνει ανοσοτροποποίηση που προκαλείται από αλλοστερική τροποποίηση του υποδοχέα άλφα-7 νικοτινικής ακετυλοχολίνης (έμμεσα ρυθμίζοντας τη δραστηριότητα των προσδεμάτων του υποδοχέα). Αν και οι ερευνητές έχουν αποδείξει αυτή τη δράση in vitro, οι συγκεντρώσεις που χρησιμοποιήθηκαν σε αυτά τα πειράματα ήταν ακόμη υψηλότερες από εκείνες που απαιτούνται για ένα αντιϊκό αποτέλεσμα [81] , και επομένως πολύ απίθανο να επιτευχθούν στον άνθρωπο. Στο μοντέλο συριακού χρυσού χάμστερ της λοίμωξης SARS-CoV-2, η ιβερμεκτίνη οδήγησε σε ορισμένες αλλαγές στον πνευμονικό ανοσοποιητικό φαινότυπο σύμφωνα με την αλλοστερική τροποποίηση του άλφα-7 νικοτινικού υποδοχέα ακετυλοχολίνης [72]. Ωστόσο, η ιβερμεκτίνη δεν φάνηκε να διασώζει την απώλεια σωματικού βάρους, η οποία είναι χαρακτηριστικό γνώρισμα της νόσου σε αυτό το μοντέλο, και οι συγκεντρώσεις του φαρμάκου δεν μετρήθηκαν ώστε να προεκταθούν σε αυτές που επιτυγχάνονται στους ανθρώπους. Συνολικά, παραμένει μεγάλη αβεβαιότητα σχετικά με τη σημασία οποιασδήποτε ανοσοτροποποιητικής ή αντιφλεγμονώδους δράσης της ιβερμεκτίνης.
Hydroxychloroquine (δημοσιεύθηκε 17 Δεκεμβρίου 2020)
Η σύσταση σχετικά με την υδροξυχλωροκίνη δημοσιεύθηκε στις 17 Δεκεμβρίου 2020 ως η τρίτη έκδοση της κατευθυντήριας γραμμής του ΠΟΥ και στο BMJ ως Ταχείες Συστάσεις . Ακολούθησε την προεκτυπωμένη δημοσίευση της δοκιμής ΑΛΛΗΛΕΓΓΥΗΣ ΠΟΥ στις 15 Οκτωβρίου 2020, η οποία ανέφερε αποτελέσματα σχετικά με τη θεραπεία με υδροξυχλωροκίνη, ρεμντεσιβίρη και λοπιναβίρη/ριτοναβίρη σε νοσηλευόμενους ασθενείς με COVID-19 [15] . Δεν έγιναν αλλαγές για τη σύσταση για την υδροξυχλωροκίνη σε αυτήν την έβδομη έκδοση της κατευθυντήριας γραμμής.
Συνιστούμε να μην χορηγείτε υδροξυχλωροκίνη ή χλωροκίνη για τη θεραπεία του COVID-19. (Ισχυρή σύσταση κατά)
Παρατήρηση: Αυτή η σύσταση ισχύει για ασθενείς με οποιαδήποτε σοβαρότητα ασθένειας και οποιαδήποτε διάρκεια συμπτωμάτων.
Λοπιναβίρη/ριτοναβίρη (δημοσιεύθηκε 17 Δεκεμβρίου 2020)
Η σύσταση σχετικά με τη λοπιναβίρη/ριτοναβίρη δημοσιεύτηκε στις 17 Δεκεμβρίου 2020 ως η τρίτη έκδοση της κατευθυντήριας γραμμής του ΠΟΥ για τη ζωή και στο BMJ ως Ταχείες Συστάσεις . Ακολούθησε την προεκτυπωμένη δημοσίευση της δοκιμής ΑΛΛΗΛΕΓΓΥΗΣ ΠΟΥ στις 15 Οκτωβρίου 2020, η οποία ανέφερε αποτελέσματα σχετικά με τη θεραπεία με λοπιναβίρη/ριτοναβιρσιβίρη, ρεμδεσιβίρη και υδροξυχλωροκίνη σε νοσηλευόμενους ασθενείς με COVID-19 [15] . Δεν έγιναν αλλαγές για τη σύσταση λοπιναβίρης/ριτοναβίρης σε αυτήν την έβδομη έκδοση της κατευθυντήριας γραμμής.
Συνιστούμε να μην χορηγήσετε λοπιναβίρη/ριτοναβίρη για τη θεραπεία του COVID-19. (Ισχυρή σύσταση κατά)
Remdesivir (δημοσιεύθηκε 20 Νοεμβρίου 2020)
Η σύσταση σχετικά με τη ρεμδεσιβίρη δημοσιεύτηκε στις 20 Νοεμβρίου 2020 ως η δεύτερη έκδοση της κατευθυντήριας γραμμής του ΠΟΥ για τη ζωή και στο BMJ ως Ταχείες Συστάσεις . Ακολούθησε την προεκτυπωμένη δημοσίευση της δοκιμής ΑΛΛΗΛΕΓΓΥΗΣ ΠΟΥ στις 15 Οκτωβρίου 2020, η οποία ανέφερε αποτελέσματα σχετικά με τη θεραπεία με ρεμντεσιβίρη, υδροξυχλωροκίνη και λοπιναβίρη/ριτοναβίρη σε νοσηλευόμενους ασθενείς με COVID-19 [15] . Δεν έγιναν αλλαγές για τη σύσταση remdesivir σε αυτήν την έβδομη έκδοση της κατευθυντήριας γραμμής.
Μηχανισμός δράσης
Το Remdesivir είναι ένα νέο προφάρμακο αναλόγου μονοφωσφοραμιδικής αδενοσίνης το οποίο μεταβολίζεται σε μια δραστική τριφωσφορική μορφή που αναστέλλει τη σύνθεση ιικού RNA. Το Remdesivir έχει in vitro και in vivo αντιική δράση έναντι αρκετών ιών, συμπεριλαμβανομένου του SARS-CoV-2. Το Remdesivir χρησιμοποιείται ευρέως σε πολλές χώρες, με αρκετές κατευθυντήριες οδηγίες που συνιστούν τη χρήση του σε ασθενείς με σοβαρό ή κρίσιμο COVID-19 [85] [86] .
Συστηματικά κορτικοστεροειδή (δημοσιεύτηκε 2 Σεπτεμβρίου 2020)
Οι συστάσεις για τα κορτικοστεροειδή δημοσιεύθηκαν για πρώτη φορά ως κατευθυντήριες οδηγίες του ΠΟΥ για τη ζωή στις 2 Σεπτεμβρίου 2020 και ως συστάσεις BMJ Rapid στις 5 Σεπτεμβρίου 2020, συμπεριλαμβανομένων συνδέσμων προς το MAGICapp. Ακολούθησε τη δημοσίευση της προκαταρκτικής έκθεσης της δοκιμής RECOVERY, η οποία δημοσιεύθηκε αργότερα ως έγγραφο με αξιολόγηση από ομοτίμους [14] . Δεν έγιναν αλλαγές για τις συστάσεις για κορτικοστεροειδή σε αυτήν την έβδομη έκδοση της κατευθυντήριας γραμμής.
Ενώ οι συστάσεις παραμένουν αμετάβλητες, η περίληψη στοιχείων για τα κορτικοστεροειδή σε ασθενείς με COVID-19 ενημερώθηκε πριν από την έκτη επανάληψη αυτής της ζωντανής κατευθυντήριας γραμμής. Οι εκτιμήσεις βασικού κινδύνου για τη θνησιμότητα βασίζονται πλέον στη δοκιμή ΑΛΛΗΛΕΓΓΥΗΣ ΠΟΥ (όπως και για άλλα φάρμακα σε αυτήν την κατευθυντήρια γραμμή) [15] αντί της αρχικής μελέτης κοόρτης ISARIC [87] που πιθανώς υπερεκτιμά τους τρέχοντες κινδύνους θνησιμότητας σε παγκόσμιο επίπεδο. Η ενημέρωση χρειαζόταν επίσης για την ενημέρωση του βασικού κινδύνου θνησιμότητας στη σύνοψη στοιχείων που ενημερώνει την ισχυρή σύσταση για αναστολείς IL-6, επιπλέον της τυπικής περίθαλψης για ασθενείς με σοβαρό ή κρίσιμο COVID-19, όπου τα κορτικοστεροειδή παρέχουν σχετική μείωση της θνησιμότητας κατά 21%.
Για ασθενείς με σοβαρό και κρίσιμο COVID-19
Συνιστούμε συστηματικά κορτικοστεροειδή παρά καθόλου κορτικοστεροειδή. (Ισχυρή σύσταση για)
Προτείνουμε να μην χρησιμοποιείτε κορτικοστεροειδή. (Σύσταση υπό όρους κατά)
ΠΟΥ Πλήρες κείμενο και συνέχεια... (κλικ εδώ)